Table des matières
Webinar du 11 juin 2020 de Roche / Genentech
Présentation des avancées du programme Angelman chez Roche / Genentech
Personnes en charge de la présentation au sein de ROCHE/GENENTECH :
- Zeena Chi, GENENTECH, en charge du lien avec les patients
- Shady Sedhom, ROCHE, lien avec les patients
- Brenda Vincenzi, ROCHE, Assistant Medical Director en charge du programme Angelman
Présentation de GENENTECH/ROCHE
ROCHE est connu aux Etats-Unis sous le nom de GENENTECH ; les deux entités ont pour but d’améliorer la vie des patients ayant des maladies sévères.

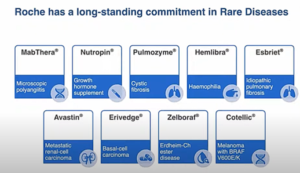
Cette diapositive présente les succès de ROCHE avec le développement de médicaments pour différentes pathologies.
Retour sur le programme Angelman
Six ans d’histoire sur l’investissement de ROCHE autour du syndrome Angelman est exposé sur cette diapositive.
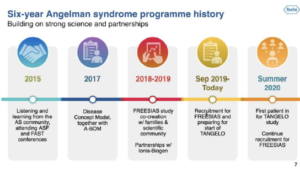
- 2015 : écoute des besoins des communautés notamment lors des conférences ASF et FAST
- 2017 : ABOM (Angelman Biomarkers and Outcome Measures) pour identifier à travers un consortium des biomarqueurs et des mesures.
- 2018-2020 : FREESIAS, définition d’une étude observationnelle
- 2020 : Lancement du programme TANGELO pour Targeting ANGELman with an Oligonucleotide.
Etude observationnelle FREESIAS
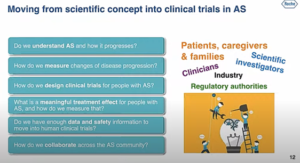
Basculer d’une preuve de concept scientifique à des essais cliniques nécessite
- D’une part, une collaboration forte entre différents acteurs (patients, soignants, familles, praticiens, scientifiques, industriels, régulateurs)
- D’autre part, de répondre ensemble à des questions importantes : compréhension de la maladie, évaluation des changements, design d’un essai clinique, analyse des données notamment sur la sécurité pour migrer vers des essais sur l’homme….

Dans le cadre d’ABOM, la question posée aux praticiens et aidants pour évaluer un essai clinique était la suivante : quelles sont les points essentiels qu’il serait critique d’étudier dans un essai clinique sur Angelman ? La réponse apportée était l’amélioration de la communication, l’autonomie, la qualité du sommeil, les compétences motrices, limiter les troubles comportementaux, réduire l’épilepsie.

FREESIAS est l’étude d’histoire naturelle qui a pour but d’affiner le design des futures études cliniques mais aussi d’avoir une cohorte de comparaison pour diminuer la taille des personnes qui auront un placebo dans des essais cliniques futures.

FREESIAS est une étude sans administration de médicament co-financée avec les laboratoires IONIS et BIOGEN.
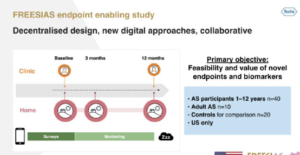
Objectifs premiers : faisabilité et identification des biomarqueurs et de certaines mesures.
Informations : 40 participants entre 1 et 12 ans et 10 adultes. Population de contrôle de 20 personnes non-AS.
FREESIAS est uniquement réalisée aux USA.
L’étude dure 12 mois avec du monitoring à la maison, des questionnaires et 2 échanges cliniques au début et à la fin du protocole.

Par exemple, l’étude va suivre des biomarqueurs avec des équipements digitaux : le sommeil avec un enregistreur, mesurer les temps des crises d’épilepsie, réaliser des EEG à la maison…
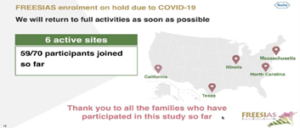
L’étude a pris du retard du fait du Covid avec un recrutement de 59/70 patients.

BIOGEN et IONIS travaillent aussi sur un médicament ASO de manière indépendante à ROCHE.
TANGELO
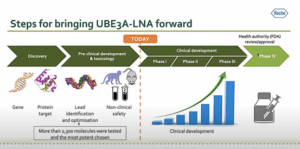
Le parcours d’un médicament avec les études précliniques puis cliniques jusqu’à la commercialisation est exposé sur cette diapositive. Actuellement, ROCHE passe en essai clinique de phase 1 avec le programme TANGELO et la molécule UBE3A-LNA choisie parmi plus de 2300 molécules testées !

UBE3A-LNA est un antisens oligonucléotide (ASO) pour agir sur le gène UBE3A dans le but de produire la protéine du même nom déficiente dans le cas du syndrome.
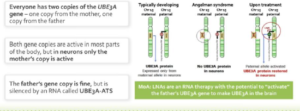
Cette dispositive présente le mécanisme de l’ASO : il vise à activer le gène UBE3A sur l’allèle paternel qui est normalement silencieux afin de permettre l’expression de la protéine UBE3A. En effet, dans le cadre du syndrome d’Angelman, la copie maternelle de ce gène située sur le chromosome 15 est non fonctionnelle et donc ne s’exprime pas.

TANGELO est une étude clinique avec plusieurs centres investigateurs dans le but d’évaluer la tolérance, la sécurité, la pharmacocinétique et pharmacodynamique liée à l’administration de l’ASO UBE3A-LNA. Dans le cadre de cet essai en phase 1, tous les patients auront une injection de l’ASO : pas de placebo ni de randomisation.
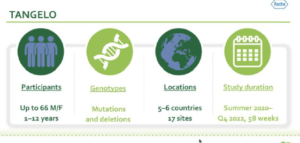
Populations : 66 hommes / femmes de 1 à 12 ans d’âge avec comme génotypes uniquement mutation ou délétion
Localisation : 5 à 6 pays avec 17 sites investigateurs
Durée de l’étude : 58 semaines s’étalant de 2020 à fin 2022 (tous les patients ne démarreront pas l’étude en même temps et donc ne la finiront pas au même moment).
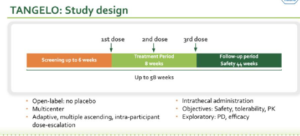
3 temps :
- 6 semaines de contrôle/screening (en orange)
- 8 semaines de traitement : 3 injections réalisées par ponction lombaire pour passer la barrière encéphalique à T0+6 semaines, T0+10 semaines, T0+14 semaines
- 44 semaines de suivi de tolérance/sécurité
Le processus de recrutement a été précisé allant des phases du consentement éclairé aux phases de critères d’inclusion / d’exclusion puis éligibilité et sélection par ROCHE. Suite au recrutement, le patient peut décider de sortir de l’étude à n’importe quel moment.
Questions/Réponses

Quels sont les critères d’exclusion dans TANGELO ?
Pour être considéré pour cette étude, il faut que tous les critères d’inclusion soient remplis et qu’aucun critère d’exclusion s’applique comme par exemple :
- Le génotype autre que délétion ou mutation
- Résultats sanguins anormaux
- Être dans un autre essai clinique
- Problème historique avec le protocole d’injection par ponction lombaire
- …

Si mon enfant est dans un autre essai clinique, combien de temps doit-il attendre avant de pouvoir être éligible dans le programme TANGELO ?
Participer à une autre étude clinique doit être approuvé par ROCHE. A la discrétion du sponsor et après discussion avec le principal investigateur, les participants peuvent être admis dans une étude observationnelle sans administration de médicaments.
Dans le cas où un participant a reçu un autre médicament, il/elle doit attendre un certain temps avant de pouvoir être dans le programme TANGELO afin que le corps se débarrasse de l’ancien médicament. Ce temps dépend des caractéristiques de l’ancien médicament et est évalué par le sponsor.

Et pour les autres génotypes ? Pourront-ils faire part de futurs essais cliniques ?
Uniquement la délétion et la mutation sont considérés dans TANGELO. Et par conséquent, le défaut d’empreinte et la disomie monoparentale ne sont pas éligibles pour des risques potentiels de surexpression de l’UBE3A lié à l’ASO et la nécessité d’avoir plus de données afin de les considérer. Néanmoins, ROCHE travaille activement aussi sur ces génotypes et les critères d’inclusion pourront différer sur les futures études cliniques après TANGELO.

Est-ce que les adultes avec le syndrome pourront bénéficier des essais ?
TANGELO a défini un critère d’inclusion d’enfants entre 1 et 12 ans. Les études sur les animaux ont montré des impacts différents en fonction de l’âge, néanmoins actuellement, ROCHE ne sait pas si cette transposition est effective chez l’homme. L’étude TANGELO sera aussi très importante en termes d’enseignements avec l’espoir d’offrir des opportunités de traitement pour tous les patients Angelman, plus ou moins âgés avec les différents génotypes.

Puis- je participer à la phase 2 et 3 si je n’ai pas participé à la phase 1 de TANGELO ?
Oui, tous les participants qui rempliront les critères d’inclusion et aucun des critères d’exclusion des futures études pourront être éligibles. Les critères d’inclusion et d’exclusion seront potentiellement différents et ne sont pas actuellement définies.

Serai-je remboursé des coûts pour participer à TANGELO ?
Les coûts d’administration liés au protocole ne sont pas à la charge du patient. Le remboursement de manière raisonnable de certains coûts (transport, nuit à l’hôtel proche du centre investigateur) sera aussi pris en charge.

Quel est l’impact du COVID sur l’essai ?
Malheureusement, la COVID a de l’impact sur de nombreux essais cliniques à travers le monde y compris FREESIAS. Il est difficile de prédire l’impact sur TANGELO car la situation varie rapidement et peut être différente d’un site investigateur à un autre. Néanmoins, ROCHE est en train de planifier le démarrage durant l’été. ROCHE en tant qu’acteur responsable met la sécurité des patients et de leurs familles au premier plan, évaluera la situation avec les sites et agira de manière appropriée.

Pourquoi les scientifiques croient que le mécanisme ASO peut être efficace ? Pourquoi celui-ci ne serait pas efficace et a-t-il été testé préalablement ?
Le mécanisme LNA (Locked Nucleid Acid) a le potentiel de modifier les principaux symptômes du syndrome en restaurant la production de la protéine UBE3A qui est défaillante au niveau neuronal.
Des études précédentes in vitro (au niveau des cellules) et in vivo (modèles animaux) ont montré que la restauration de la protéine manquante se traduit par une restauration du phénotype. Ce mécanisme n’a pas été testé sur l’humain avant et bien que ROCHE n’ait pas de raison de croire qu’il pourrait ne pas être efficace, la société ne peut prédire avec certitude que les résultats observés sur les modèles animaux soient complètement transférables à l’homme.

Quels symptômes associés à Angelman pourra être adressé par ce médicament ?
UBE3A-LNA permet de retirer le « stop » de la copie du père qui est naturellement silencieuse dans le but de permettre la production de la protéine manquante dans le cerveau des individus atteints par le syndrome.
UBE3A-LNA a le potentiel de modifier la maladie en adressant tous les symptômes du syndrome. C’est différent d’un médicament qui va soigner uniquement un symptôme comme par exemple pour contrôler l’épilepsie ou améliorer le sommeil.

Pour les familles qui ne sont pas dans l’étude FREESIAS ou à venir TANGELO, comment rester au courant de ce qui se passe ?
La communication pour ROCHE est clé avec la communauté et l’information sera accessible à tous.

Vous pourrez également consulter le protocole à cette adresse. FAST France vous fera l’écho des avancées.
Y a-t-il des effets indésirables liés à la thérapie ?
Durant la phase de sélection du médicament, ROCHE a déterminé la molécule la plus prometteuse mais aussi ayant la sécurité la plus forte. Dans le cas des essais précliniques sur les animaux, le médicament était très bien toléré et l’équipe s’attend à peu d’effets indésirables et monitore les patients dans le cas des essais cliniques pour les effets indésirables.
Si mon enfant a eu des complications mais qu’il va bien maintenant, peut-il participer à l’essai ?
La réponse n’est pas simple et demande des informations plus précises sur les antécédents du patient. S’il remplit les critères d’inclusion sans aucun critère d’exclusion, alors il est éligible. Les centres investigateurs souhaitent avant tout protéger la sécurité des patients et évaluer le traitement sans des facteurs préalables.
Est-ce que mon enfant peut être à la fois dans FREESIAS et TANGELO ?
La réponse est non. Il faut stopper FREESIAS afin d’être dans le programme TANGELO car les deux études ont des objectifs différents.
Est-ce qu’il va y avoir des mesures d’efficacité dans le cadre de TANGELO ?
Dans le cadre du programme TANGELO, l’efficacité est exploratoire et il n’y a pas d’efficacité finale prédéfinie. TANGELO ainsi que FREESIAS contribueront à développer des mesures d’efficacité pour les futurs essais cliniques.
Le compte-rendu de FAST France a été établi à partir du webinar que vous pouvez retrouver : www.Angelmanclinicaltrials.com/industrysponsors
Disclaimer : FAST France a participé au webinar au webinar public donné par la société ROCHE le 11 Juin 2020 et met à disposition de la communauté francophone ce compte rendu pour information. En cas de divergence imputable à une erreur de traduction ou de compréhension, uniquement le webinar en anglais réalisé par ROCHE prévaut sur le compte-rendu. En aucun cas, FAST France ne pourra être tenu pour responsable de ces erreurs.