FAST France partage les dernières informations communiquées par le laboratoire Roche revenant sur le programme Aldebaran et la molécule Alogabat.
Vous trouverez ci-joint le document transmis par le laboratoire avec le programme Aldebaran.
Design initial du programme Aldebaran, il y aura jusqu’à 7 cohortes. Les adolescents âgés de 15 à 17 ans recevront la dose adulte. Le dosage dans la partie 1 est pré-spécifié. Les cohortes de la partie 1 incluent une tranche d’âge spécifique (15-17 ans, 10-14 ans, 5-9 ans), les cohortes plus âgées étant initiées avant les plus jeunes.
La partie 2 comprend des cohortes d’âges différents, avec des doses ajustées en fonction de l’âge. Dans chaque cohorte de la partie 2, deux doses différentes d’alogabat peuvent être utilisées : l’une jusqu’à la semaine 2, et l’autre de la semaine 2 à la semaine 12. La partie 2 ouvre les inscriptions pour les 10-17 ans après l’analyse des données à 2 semaines des cohortes de la partie 1 âgées de 15-17 ans et de 10-14 ans. Les participants âgés de 5 à 9 ans peuvent s’inscrire à la partie 2 après analyse des données de deux semaines de la cohorte de la partie 1 dont les participants sont âgés de 5 à 9 ans. Au total, deux cohortes facultatives peuvent être utilisées dans cette étude, réparties entre la partie 1 et/ou la partie 2.
Au niveau réglementaire, le laboratoire Roche a soumis la version 2 du protocole le 13 juillet dernier et a obtenu l’autorisation pour ce protocole au mois d’octobre. L’impact majeur de cette version du protocole est de permettre une ouverture moins séquentielle des parties et des cohortes de l’étude.
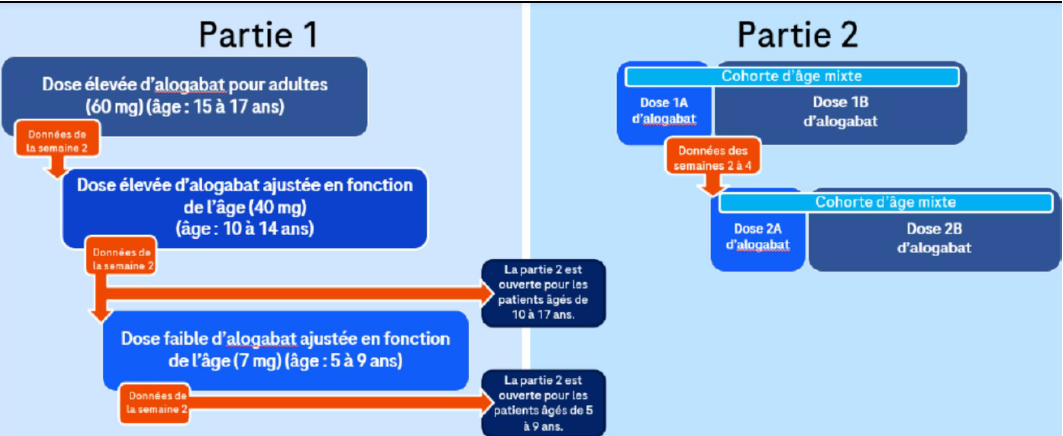
Design modifié du protocole
Pour résumer, la Partie 2 pourra ouvrir dès que la laboratoire aura analysé les informations liées à la sécurité d’emploi du produit des cohortes 15-17 ans et 10-14 ans de la Partie 1. Il était initialement prévu d’attendre que toutes les cohortes de la Partie 1 soient analysées avant d’ouvrir celles de la Partie 2.
Au niveau du recrutement, au niveau international, 1 patient a complété sa phase de traitement et termine bientôt sa phase de suivi. 2 patients sont en cours de suivi et 1 patient est en cours de screening. Le laboratoire Roche espère pouvoir démarrer le screening du premier patient Français avant la fin de l’année. L’étude au niveau mondial devrait enrôler 56 patients.
Points de contact pour les essais sur Aldebaran au niveau des centres investigateurs :
- AP HP Necker/Imagine: contact-essaisangelman@institutimagine.org
- AP HM CHU de Marseille/La Timone : RDV-neuropediatrie.timoneenfants@aphm.fr
- CHRU Brest : consultations.piedatrie@chu-brest.fr
Pour en savoir plus sur le programme Aldebaran et le principe d’action d’Alogabat, nous vous renvoyons vers le post suivant.